ANTIOXIDÁNS TULAJDONSÁGÚ
NÖVÉNYI HATÓANYAGOK. A FLAVONOIDOK
1. Bevezetés
A növényi flavonoidok szerepéről, kémiai
szerkezetéről, élettani hatásáról az elmúlt negyven évben rendszeresen jelentek
meg összefoglaló tanulmányok (2, 7, 8), de az emberi szervezetre gyakorolt
hatásuk és jelentőségük még ma sem teljesen tisztázott. A flavonoidok az
élelmiszerek nem tápanyag komponensei, vagyis nem jelentenek tápértéket az
emberi szervezet számára. Szent- Györgyi és munkatársai már 1936-ban kimutatták,
hogy a citrusfélékből származó két flavonoid (rutin, naringenin) csökkenti a
kapillárisok törékenységét és permeabilitását (21). Ezért a flavonoidokat
P-vitaminnak nevezte el (P - permeabilitás), illetve C 2 -vitaminnak, mivel
számos flavonoid képes a C-vitamint stabilizálni. Később a flavonoidok vitamin
elmélete megdőlt, és az `50-es években mindkét elnevezést elvetették. A hetvenes
években felfedezték, hogy a növényekben az egyik leggyakrabban előforduló
flavonoid, a kvercetin bizonyos körülmények között mutagén hatású, ezért nagy
figyelem irányult a flavonoidok karcinogenitására, amelyet később nem sikerült
egyértelműen bizonyítani. Napjainkban e korai eredményeket kissé elfelejtve a
legtöbb kutatócsoport a flavonoidok antioxidáns, antikarcinogén és
gyulladáscsökkentő, összességében egészségvédő és betegségmegelőző hatását
helyezi előtérbe.
2. A flavonoidok kémiai szerkezete, előfordulásuk
A flavonoidokra
a C 6 -C 3 -C 6 alapszénváz jellemző, a két benzolgyűrű egy oxigénatomot
tartalmazó heterociklikus pirán- vagy pirongyűrűn keresztül kapcsolódik (1.
ábra).
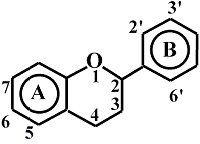 Ez az alapszerkezet rendkívüli változatosságot biztosít mind a szubsztituensek,
mind a C-gyűrű szerkezete tekintetében. Jelenleg mintegy 4000-féle különböző
szerkezetű flavonoidot azonosítottak (2, 6). Az alapvázhoz (aglikon) különböző
cukormolekulák kapcsolódhatnak, és glükozidokat hoznak létre, amelyek sokkal
gyakrabban fordulnak elő a természetben, mint aglikonjaik. A flavonoidokon 13
különböző vegyületcsoportot értünk, amelyek egymástól az alapszerkezethez
kapcsolódó hidroxilcsoportok számában, helyzetében, valamint a C 2 - C 3
szénatomok közötti kettős kötés meglétében vagy hiányában térnek el egymástól.
Néhány vegyület fontos egészségvédő szerepet játszhat, mint a flavanonok,
flavonok, flavonolok, flavanok, antociánok és izoflavonok, míg az egyéb
flavonoid komponensek, mint az auronok, chalconok és kumarinok szerepe jelenlegi
ismereteink szerint kevésbé jelentős. nem valamennyi növényi élelmiszerben
megtalálhatók a mg/kg koncentrációtól egészen a néhány g/kg tartományig. A
legtöbb ital, amely természetes növényi alkotórészből készül (zöldség- és
gyümölcslevek, gyógyteák) kisebb-nagyobb mennyiségben tartalmaz flavonoidokat,
polifenolos vegyületeket (2, 9). Saját vizsgálatainkban öt, a természetben
leggyakrabban előforduló flavonoidvegyület, a kvercetin, a luteolin, az
apigenin, a kempferol és a miricetin mennyiségét határoztuk meg mintegy 150-féle
növényi élelmiszerben (17, 19). Az összes flavonoid mennyiségét illetően a
zöldségek közül a hagymafélék, a fehérrépa, a spenót, a zeller különböző részei
és a különböző lencsefajták bizonyultak a leggazdagabb forrásnak. A gyümölcsök
közül jelentős flavonoidforrások a bogyósok, az olajos magvak közül pedig a dió
tűnt ki nagyon jelentős flavonoidtartalmával. Az egyes flavonoid vegyületek
közül nagy mennyiségű kvercetin volt kimutatható a vörös- és lilahagymában, a
sóskában és a spenótban. A miricetin koncentrációban volt kimutatható a dióban,
az eperben, a szederben, a fehérrépában és a petrezselyemzöldben
Ez az alapszerkezet rendkívüli változatosságot biztosít mind a szubsztituensek,
mind a C-gyűrű szerkezete tekintetében. Jelenleg mintegy 4000-féle különböző
szerkezetű flavonoidot azonosítottak (2, 6). Az alapvázhoz (aglikon) különböző
cukormolekulák kapcsolódhatnak, és glükozidokat hoznak létre, amelyek sokkal
gyakrabban fordulnak elő a természetben, mint aglikonjaik. A flavonoidokon 13
különböző vegyületcsoportot értünk, amelyek egymástól az alapszerkezethez
kapcsolódó hidroxilcsoportok számában, helyzetében, valamint a C 2 - C 3
szénatomok közötti kettős kötés meglétében vagy hiányában térnek el egymástól.
Néhány vegyület fontos egészségvédő szerepet játszhat, mint a flavanonok,
flavonok, flavonolok, flavanok, antociánok és izoflavonok, míg az egyéb
flavonoid komponensek, mint az auronok, chalconok és kumarinok szerepe jelenlegi
ismereteink szerint kevésbé jelentős. nem valamennyi növényi élelmiszerben
megtalálhatók a mg/kg koncentrációtól egészen a néhány g/kg tartományig. A
legtöbb ital, amely természetes növényi alkotórészből készül (zöldség- és
gyümölcslevek, gyógyteák) kisebb-nagyobb mennyiségben tartalmaz flavonoidokat,
polifenolos vegyületeket (2, 9). Saját vizsgálatainkban öt, a természetben
leggyakrabban előforduló flavonoidvegyület, a kvercetin, a luteolin, az
apigenin, a kempferol és a miricetin mennyiségét határoztuk meg mintegy 150-féle
növényi élelmiszerben (17, 19). Az összes flavonoid mennyiségét illetően a
zöldségek közül a hagymafélék, a fehérrépa, a spenót, a zeller különböző részei
és a különböző lencsefajták bizonyultak a leggazdagabb forrásnak. A gyümölcsök
közül jelentős flavonoidforrások a bogyósok, az olajos magvak közül pedig a dió
tűnt ki nagyon jelentős flavonoidtartalmával. Az egyes flavonoid vegyületek
közül nagy mennyiségű kvercetin volt kimutatható a vörös- és lilahagymában, a
sóskában és a spenótban. A miricetin koncentrációban volt kimutatható a dióban,
az eperben, a szederben, a fehérrépában és a petrezselyemzöldben
(1.
táblázat).
1. táblázat: növényi élelmiszerek flavonoidtartalma (mg/kg)
| Minta |
KVE |
KEM |
MIR |
LUT |
API |
Összes |
| Zöldségek |
| Brokkoli |
15,4 |
30,8 |
nd a |
nd |
nd |
46,2 |
| Karalábé |
4,0 |
24,3 |
nd |
13,0 |
nd |
41,3 |
| Fehér káposzta |
1,6 |
11,9 |
nd |
4,2 |
nd |
17,7 |
| Vöröshagyma |
121,5 |
2,6 |
nd |
nd |
nd |
124,1 |
| Lilahagyma |
171,3 |
24,3 |
nd |
nd |
nd |
195,6 |
| Paprika |
9,4 |
nd |
nd |
10,7 |
nd |
20,1 |
| Fodros saláta |
35,0 |
8,4 |
nd |
3,9 |
nd |
47,3 |
| Spenót |
272,2 |
nd |
nd |
66,4 |
nd |
338,6 |
| Zellerzöld |
nd |
nd |
43,4 |
111,4 |
248 |
402,8 |
| Zellergyökér |
1,8 |
nd |
nd |
nd |
24,1 |
25,9 |
| Fehérrépa |
3,2 |
22,7 |
85,4 |
nd |
154,0 |
265,3 |
| Torma |
5,7 |
25,7 |
nd |
9,0 |
nd |
40,4 |
| Gyümölcsök |
| Alma |
38,3 |
nd |
nd |
nd |
27,0 |
65,3 |
| Körte |
24,7 |
nd |
nd |
nd |
nd |
24,7 |
| Görögdinnye |
nd |
nd |
nd |
nd |
18,4 |
18,4 |
| Sárgadinnye |
nd |
nd |
nd |
nd |
25,8 |
25,8 |
| Szilva |
23,3 |
nd |
nd |
nd |
nd |
23,3 |
| Sárgabarack |
11,5 |
nd |
nd |
nd |
nd |
11,5 |
| Meggy |
29,2 |
nd |
nd |
nd |
nd |
29,2 |
| Szeder |
14,0 |
nd |
636 |
nd |
nd |
650 |
| Eper |
9,0 |
nd |
994 |
nd |
nd |
1003 |
| Dió |
nd |
nd |
4565 |
nd |
nd |
4565 |
| Kivi |
nd |
nd |
nd |
nd |
22,3 |
22,3 |
| Banán |
nd |
nd |
22,8 |
nd |
nd |
22,8 |
a : nd - kimutatási határ alatt
KVE - kvercetin, KEM - kempferol, MIR -
miricetin, LUT - luteolin, API - apigenin
3. Étrendi felvétel és epidemiológiai összefüggések
Kühnau a
`70-es években az amerikai lakosság összes polifenolfelvételét az izoflavonoidok
kivételével az 5 fő flavonoidcsoportba tartozó vegyületekből 1-1,1 g/nap körüli
értékben határozta meg, ebből 115 mg a flavonol és flavon (15). A holland
lakosság napi flavonoidfelvétele 23 mg-nak bizonyult, míg Leth és Justesen a
dánok felvételetelét 28 mg/nap értéknek találta (10, 1. ábra: a flavonoidok
alapszerkezete A flavonoidok a növényi metabolizmus másodlagos termékei. Számos
funkciójuk ismert a növényvilágban: pigmentálás, az UV-fény, a mikroorganizmusok
és egyéb növényi kártevők - gombák, rovarok, csigák stb. - elleni védelem. Az
élelmiszerként szolgáló növényi anyagokban természetes színezőanyagok,
ízkomponensek, antioxidánsok (7, 8, 15). A flavonoidok csak16). A finn lakosság
flavonoidfelvétele 55,2 mg/nap (14). Hazai vizsgálatok szerint a magyar gyerekek
átlagos flavonoidfelvétele 19,5 ± 26,6 mg/fő érték, míg a felnőttek által
elfogyasztott flavonoid mennyisége 18,8 ± 28,9 mg/ fő volt. A számított értékek
nagy egyénenkénti változatosságot mutattak, gyerekek esetében a felvétel 0-179,3
mg, felnőtteknél 0,5-309,7 mg között változott (18).
![Kép helye]() A ''Seven Country Study''-ban a szerzők a 25 éves követéses vizsgálat
eredményei alapján arra a megállapításra jutottak, hogy a flavonoidfelvétel
inverz módon összefügg a szívés érrendszeri betegségekkel összefüggésbe hozható
mortalitással (11). A Zutphen (Hollandia) tanulmányban a flavonoidfelvétel
inverz összefüggésben volt az ötéves követéses időszakban megjelenő daganatos és
koronáriás betegségek számával. A szív- és érrendszeri betegségekből származó
mortalitás 50%-kal kisebb volt a legnagyobb flavonoidfelvételű csoportban a
legkevesebbet fogyasztókhoz viszonyítva. A flavonoidfelvétel nem befolyásolta a
daganatos betegségek morbiditását és mortalitását (10). Egy 1996-ban megjelent
finn tanulmányban a nők esetében szignifikáns inverz összefüggés volt
kimutatható a flavonoidfelvétel és az összes, valamint a koronáriás
szívbetegségekből eredő halálozások tekintetében is. A férfiak esetében ugyanezt
a trendet sikerült kimutatni, de csak az összes halálozásra vonatkozóan volt
szignifikáns az összefüggés (13).
A ''Seven Country Study''-ban a szerzők a 25 éves követéses vizsgálat
eredményei alapján arra a megállapításra jutottak, hogy a flavonoidfelvétel
inverz módon összefügg a szívés érrendszeri betegségekkel összefüggésbe hozható
mortalitással (11). A Zutphen (Hollandia) tanulmányban a flavonoidfelvétel
inverz összefüggésben volt az ötéves követéses időszakban megjelenő daganatos és
koronáriás betegségek számával. A szív- és érrendszeri betegségekből származó
mortalitás 50%-kal kisebb volt a legnagyobb flavonoidfelvételű csoportban a
legkevesebbet fogyasztókhoz viszonyítva. A flavonoidfelvétel nem befolyásolta a
daganatos betegségek morbiditását és mortalitását (10). Egy 1996-ban megjelent
finn tanulmányban a nők esetében szignifikáns inverz összefüggés volt
kimutatható a flavonoidfelvétel és az összes, valamint a koronáriás
szívbetegségekből eredő halálozások tekintetében is. A férfiak esetében ugyanezt
a trendet sikerült kimutatni, de csak az összes halálozásra vonatkozóan volt
szignifikáns az összefüggés (13).
4. A flavonoidok kémiaibiokémiai tulajdonságai
A flavonoidok igen
széles körű kémiai és biológiai aktivitással rendelkeznek. A részben vagy
teljesen bizonyított hatások meglehetősen szerteágazók. Az in vitro, valamint az
utóbbi öt évben megsokszorozódott in vivo vizsgálatok alapján a flavonoidok
kedvező hatásai a következő biokémiai folyamatok köré csoportosíthatók: 1)
antioxidáns hatás és/vagy szabadgyök-befogás, 2) immunmoduláns és
gyulladáscsökkentő hatás - nagy valószínűséggel az arachidonsav-metabolizmus
módosításán keresztül, 3) asztmaellenes és antiallergén hatás, 4) más enzimek
aktivitásának módosítása, általában gátlása, 5) antivirális, antibakteriális
hatás, 6) ösztrogénaktivitás (izoflavonoidok), 7) mutagenezist és
karcinogenezist befolyásoló hatás, 8) hepatoprotektív hatás, 9) véredényrendszer
működését, állapotát befolyásoló hatás, vaszkuláris permeabilitás módosítása. A
fenti tulajdonságok több esetben egymással összefüggnek: a hepatoprotektív hatás
a szabadgyökbefogó tulajdonsággal, az antioxidáns hatás sok esetben a
xantinoxidáz-gátlással, az asztmaellenes hatás az 5lipoxigenáz-gátlással (2, 5,
16, 20). A fenolos antioxidánsok szabadgyök terminátorként és fémionkelátorként
funkcionálhatnak. Hidrogénatomot átadva a szabad gyökök bekapcsolódnak a lipidek
és egyéb molekulák oxidációs folyamataiba. A keletkezett átmeneti termék, a
fenoxigyök relatíve stabil molekula, ezért az újabb láncreakció iniciációja
nehezen következik be. A fenoxigyök más szabad gyökökkel reagálva részt vesz a
láncreakció terminációjában. A flavonoidok antioxidáns tulajdonságainak mértéke
alapvetően az adott molekula szerkezetétől függ (1, 2, 12).
Az irodalmi
adatok szerint a flavonoidok relatíve nem toxikusak a magasabb rendű állatok és
az ember számára, eddig teratogén hatást sem sikerült kimutatni. Az Ames-féle in
vitro Salmonella typhimurium short-term mutagenezis tesztben számos flavonoid
mutagénnek bizonyult, mikroszomális (S-9) metabolikus aktiváció mellett és annak
hiányában is (3, 4). A kvercetin több in vitro short-term kísérletben
genotoxikus hatású volt emlős sejtvonalakon. Több kutatócsoport tett kísérletet
a flavonoidok in vivo genotoxikus hatásának bizonyítására, de legtöbbjük kevés
sikerrel járt. Az ezen a területen munkálkodó kutatók összegzése szerint a
flavonoidok antikarcinogén hatása sokkal jelentősebb, mint azok prokarcinogén
tulajdonságai, de ez utóbbi sem elhanyagolható. A tisztán növényi étrendet
fogyasztó vegetárius egyének esetében az eddig elvégzett vizsgálatok nem
mutattak ki negatív hatást a vegyes étrenden élőkhöz viszonyított jelentősen
nagyobb flavonoidfelvétellel összefüggésben.
5. Problémák az étrendi eredetű flavonoidok táplálkozás-élettani
megítélésében
A flavonoidok a gasztrointesztinális szakaszban
kisebb-nagyobb szerkezetátalakuláson mennek át. Feltételezhető az is, hogy a
szervezetben a felszívódás után teljesen más metabolitok vannak jelen, mint az
emésztést megelőzően. Ezért a flavonoidok táplálkozás-élettani hatásai nem
szükségszerűen a flavonoidoknak tulajdoníthatók, hanem az enterális és
posztabszorpciós interakciók és degradációs folyamatok során keletkező
metabolitoknak. Ezért éles határvonalat kell húzni az in vitro és invivo
vizsgálati eredmények között, valamint az orálisan vagy más úton a szervezetbe
juttatott flavonoidok hatásai között is. Nem vethető el az a lehetőség sem, hogy
a flavonoidok élettani hatását alapvetően az határozza meg, mi történik a
bélrendszerben, és hogy van-e és ha igen, akkor milyen kapcsolat az
immunrendszer, az intesztinum baktériumai és a flavonoidok között.
![Kép helye]() Az étrendi flavonoidok más élelmiszer-alkotókkal együtt
jutnak a szervezetbe, ezért hatásukat a kísérő, ill. jelen lévő egyéb
komponensekkel történő kölcsönhatások is befolyásolják. A flavonoidok hatása
jelenlegi ismereteink szerint főleg preventív (megelőző). Napjainkban a
flavonoidok és az egyéb polifenolos vegyületek egyre inkább a tudományos
kutatások előterébe kerülnek, mint olyan étrendi komponensek, amelyek rendkívül
fontos szerepet játszanak a betegségek megelőzésében és az egészség
megőrzésében. Pozitív élettani hatásukban alapvető fontosságú, de nem
kizárólagos szerepet játszik bizonyított antioxidáns tulajdonságuk. Élettani
hatásuk pontos megismeréséhez sokkal több és megbízható, tudományosan igazolt
információra van szükségünk az élelmiszerekben előforduló flavonoidok
koncentrációjáról, a konyhatechnikai és egyéb technológiai folyamatok során
bekövetkező átalakulásokról és veszteségekről, valamint újabb epidemiológiai
tanulmányok is elengedhetetlenül szükségesek. Fentiek miatt a flavonoidok
növényi élelmiszerekkel történő rendszeres fogyasztását messzemenően javasoljuk,
amely akár a vegetárius étrend határáig is terjedhet, ugyanakkor a nagy dózisú
étrendkiegészítőkkel történő, hosszan tartó felvételt a potenciális
egészségkárosító hatások elkerülése érdekében elkerülendőnek tartjuk.
Az étrendi flavonoidok más élelmiszer-alkotókkal együtt
jutnak a szervezetbe, ezért hatásukat a kísérő, ill. jelen lévő egyéb
komponensekkel történő kölcsönhatások is befolyásolják. A flavonoidok hatása
jelenlegi ismereteink szerint főleg preventív (megelőző). Napjainkban a
flavonoidok és az egyéb polifenolos vegyületek egyre inkább a tudományos
kutatások előterébe kerülnek, mint olyan étrendi komponensek, amelyek rendkívül
fontos szerepet játszanak a betegségek megelőzésében és az egészség
megőrzésében. Pozitív élettani hatásukban alapvető fontosságú, de nem
kizárólagos szerepet játszik bizonyított antioxidáns tulajdonságuk. Élettani
hatásuk pontos megismeréséhez sokkal több és megbízható, tudományosan igazolt
információra van szükségünk az élelmiszerekben előforduló flavonoidok
koncentrációjáról, a konyhatechnikai és egyéb technológiai folyamatok során
bekövetkező átalakulásokról és veszteségekről, valamint újabb epidemiológiai
tanulmányok is elengedhetetlenül szükségesek. Fentiek miatt a flavonoidok
növényi élelmiszerekkel történő rendszeres fogyasztását messzemenően javasoljuk,
amely akár a vegetárius étrend határáig is terjedhet, ugyanakkor a nagy dózisú
étrendkiegészítőkkel történő, hosszan tartó felvételt a potenciális
egészségkárosító hatások elkerülése érdekében elkerülendőnek tartjuk.
Lugasi Andrea főosztályvezető-helyettes
Fodor
József Országos Közegészségügyi Központ Országos Élelmezés- és
Táplálkozástudományi Intézete, Budapest
Hivatkozások
1. Bors, W., Heller, W., Michel, C., Saran, M., Meth.
Enzymol., 186. 343-355. 1990.
2. Bravo, L., Nutr. Rev., 56. 317-333. 1998.
3. Brown, J. P., Dietrich, P. S., Mutat. Res., 66. 223-240. 1979.
4.
Czeczot, H., Tudek, B., Kusztelak, J. és mtsai, Mutat. Res., 240. 209- 216.
1990.
5. Duthie, G. G., Crozier, A., Curr. Opin. Lipid., 11. 43-47. 2000.
6. Duthie, G. G., Duthie, S. J., Kyle, J. A., Nutr. Res. Rev., 13. 79-106.
2000.
7. Harborne, J. B., Prog. Clin. Biol. Res., 213. 15-24. 1986.
8.
Herrman, K., J. Food Technol., 11. 433-448. 1976.
9. Hertog, M. G. L.,
Hollman, P. C. H., Katan, M. B., J. Agric. Food Chem., 40. 2379-2383. 1992.
10. Hertog, M. G. L:, Feskens, E. J. M., Hollman, P. C. és mtsai, Lancet,
342. 1007-1011. 1993.
11. Hertog, M. G. L., Kromhout, D., Aravanis, C. és
mtsai, Arch. Intern. Med., 155. 381-386. 1995.
12. Kandaswami, C.,
Middleton, E., Adv. Exp. Med. Biol., 366. 351- 376. 1994.
13. Knekt, P.,
Järvinen, R., Reunanen, A. és mtsa, Br. Med. J., 312. 478- 481. 1996.
14.
Kumpulainen, J. T., Lehtonen, M., Mattila, P. In: Natural Antioxidants and
anticarcinogens in nutrition, health and disease. (Ed.: Kumpulainen, J. T.,
Salonen, J. T.), RSC, Cambridge, UK, 141-150. 1999.
15. Kühnau, J., World
Rev. Nutr. Diet, 24. 117-120. 1976.
16. Leth, T., Justesen, U. In:
Polyphenols in food. (Eds.: Amado, R., Andersson, H., Bardócz, S., Serra, F.)
EU, pp. 39-40. 1998.
17. Lugasi, A., Hóvári, J., Acta Alim. 29. 345-352.
2000.
18. Lugasi A., Hóvári J., Sági V. K., Bíró L., Egészségtudomány, 45.
3. 244- 255. 2001.
19. Lugasi, A., Hóvári, J., Acta Alim., 31. 63-71. 2002.
20. Peterson, J., Dwyer, J., Nutr. Res., 18. 1995-2019. 1998.
21.
Rusznyák, S., Szent-Györgyi, A., Nature, 138. 798. 1936.
 Ez az alapszerkezet rendkívüli változatosságot biztosít mind a szubsztituensek,
mind a C-gyűrű szerkezete tekintetében. Jelenleg mintegy 4000-féle különböző
szerkezetű flavonoidot azonosítottak (2, 6). Az alapvázhoz (aglikon) különböző
cukormolekulák kapcsolódhatnak, és glükozidokat hoznak létre, amelyek sokkal
gyakrabban fordulnak elő a természetben, mint aglikonjaik. A flavonoidokon 13
különböző vegyületcsoportot értünk, amelyek egymástól az alapszerkezethez
kapcsolódó hidroxilcsoportok számában, helyzetében, valamint a C 2 - C 3
szénatomok közötti kettős kötés meglétében vagy hiányában térnek el egymástól.
Néhány vegyület fontos egészségvédő szerepet játszhat, mint a flavanonok,
flavonok, flavonolok, flavanok, antociánok és izoflavonok, míg az egyéb
flavonoid komponensek, mint az auronok, chalconok és kumarinok szerepe jelenlegi
ismereteink szerint kevésbé jelentős. nem valamennyi növényi élelmiszerben
megtalálhatók a mg/kg koncentrációtól egészen a néhány g/kg tartományig. A
legtöbb ital, amely természetes növényi alkotórészből készül (zöldség- és
gyümölcslevek, gyógyteák) kisebb-nagyobb mennyiségben tartalmaz flavonoidokat,
polifenolos vegyületeket (2, 9). Saját vizsgálatainkban öt, a természetben
leggyakrabban előforduló flavonoidvegyület, a kvercetin, a luteolin, az
apigenin, a kempferol és a miricetin mennyiségét határoztuk meg mintegy 150-féle
növényi élelmiszerben (17, 19). Az összes flavonoid mennyiségét illetően a
zöldségek közül a hagymafélék, a fehérrépa, a spenót, a zeller különböző részei
és a különböző lencsefajták bizonyultak a leggazdagabb forrásnak. A gyümölcsök
közül jelentős flavonoidforrások a bogyósok, az olajos magvak közül pedig a dió
tűnt ki nagyon jelentős flavonoidtartalmával. Az egyes flavonoid vegyületek
közül nagy mennyiségű kvercetin volt kimutatható a vörös- és lilahagymában, a
sóskában és a spenótban. A miricetin koncentrációban volt kimutatható a dióban,
az eperben, a szederben, a fehérrépában és a petrezselyemzöldben
Ez az alapszerkezet rendkívüli változatosságot biztosít mind a szubsztituensek,
mind a C-gyűrű szerkezete tekintetében. Jelenleg mintegy 4000-féle különböző
szerkezetű flavonoidot azonosítottak (2, 6). Az alapvázhoz (aglikon) különböző
cukormolekulák kapcsolódhatnak, és glükozidokat hoznak létre, amelyek sokkal
gyakrabban fordulnak elő a természetben, mint aglikonjaik. A flavonoidokon 13
különböző vegyületcsoportot értünk, amelyek egymástól az alapszerkezethez
kapcsolódó hidroxilcsoportok számában, helyzetében, valamint a C 2 - C 3
szénatomok közötti kettős kötés meglétében vagy hiányában térnek el egymástól.
Néhány vegyület fontos egészségvédő szerepet játszhat, mint a flavanonok,
flavonok, flavonolok, flavanok, antociánok és izoflavonok, míg az egyéb
flavonoid komponensek, mint az auronok, chalconok és kumarinok szerepe jelenlegi
ismereteink szerint kevésbé jelentős. nem valamennyi növényi élelmiszerben
megtalálhatók a mg/kg koncentrációtól egészen a néhány g/kg tartományig. A
legtöbb ital, amely természetes növényi alkotórészből készül (zöldség- és
gyümölcslevek, gyógyteák) kisebb-nagyobb mennyiségben tartalmaz flavonoidokat,
polifenolos vegyületeket (2, 9). Saját vizsgálatainkban öt, a természetben
leggyakrabban előforduló flavonoidvegyület, a kvercetin, a luteolin, az
apigenin, a kempferol és a miricetin mennyiségét határoztuk meg mintegy 150-féle
növényi élelmiszerben (17, 19). Az összes flavonoid mennyiségét illetően a
zöldségek közül a hagymafélék, a fehérrépa, a spenót, a zeller különböző részei
és a különböző lencsefajták bizonyultak a leggazdagabb forrásnak. A gyümölcsök
közül jelentős flavonoidforrások a bogyósok, az olajos magvak közül pedig a dió
tűnt ki nagyon jelentős flavonoidtartalmával. Az egyes flavonoid vegyületek
közül nagy mennyiségű kvercetin volt kimutatható a vörös- és lilahagymában, a
sóskában és a spenótban. A miricetin koncentrációban volt kimutatható a dióban,
az eperben, a szederben, a fehérrépában és a petrezselyemzöldben  A ''Seven Country Study''-ban a szerzők a 25 éves követéses vizsgálat
eredményei alapján arra a megállapításra jutottak, hogy a flavonoidfelvétel
inverz módon összefügg a szívés érrendszeri betegségekkel összefüggésbe hozható
mortalitással (11). A Zutphen (Hollandia) tanulmányban a flavonoidfelvétel
inverz összefüggésben volt az ötéves követéses időszakban megjelenő daganatos és
koronáriás betegségek számával. A szív- és érrendszeri betegségekből származó
mortalitás 50%-kal kisebb volt a legnagyobb flavonoidfelvételű csoportban a
legkevesebbet fogyasztókhoz viszonyítva. A flavonoidfelvétel nem befolyásolta a
daganatos betegségek morbiditását és mortalitását (10). Egy 1996-ban megjelent
finn tanulmányban a nők esetében szignifikáns inverz összefüggés volt
kimutatható a flavonoidfelvétel és az összes, valamint a koronáriás
szívbetegségekből eredő halálozások tekintetében is. A férfiak esetében ugyanezt
a trendet sikerült kimutatni, de csak az összes halálozásra vonatkozóan volt
szignifikáns az összefüggés (13).
A ''Seven Country Study''-ban a szerzők a 25 éves követéses vizsgálat
eredményei alapján arra a megállapításra jutottak, hogy a flavonoidfelvétel
inverz módon összefügg a szívés érrendszeri betegségekkel összefüggésbe hozható
mortalitással (11). A Zutphen (Hollandia) tanulmányban a flavonoidfelvétel
inverz összefüggésben volt az ötéves követéses időszakban megjelenő daganatos és
koronáriás betegségek számával. A szív- és érrendszeri betegségekből származó
mortalitás 50%-kal kisebb volt a legnagyobb flavonoidfelvételű csoportban a
legkevesebbet fogyasztókhoz viszonyítva. A flavonoidfelvétel nem befolyásolta a
daganatos betegségek morbiditását és mortalitását (10). Egy 1996-ban megjelent
finn tanulmányban a nők esetében szignifikáns inverz összefüggés volt
kimutatható a flavonoidfelvétel és az összes, valamint a koronáriás
szívbetegségekből eredő halálozások tekintetében is. A férfiak esetében ugyanezt
a trendet sikerült kimutatni, de csak az összes halálozásra vonatkozóan volt
szignifikáns az összefüggés (13).  Az étrendi flavonoidok más élelmiszer-alkotókkal együtt
jutnak a szervezetbe, ezért hatásukat a kísérő, ill. jelen lévő egyéb
komponensekkel történő kölcsönhatások is befolyásolják. A flavonoidok hatása
jelenlegi ismereteink szerint főleg preventív (megelőző). Napjainkban a
flavonoidok és az egyéb polifenolos vegyületek egyre inkább a tudományos
kutatások előterébe kerülnek, mint olyan étrendi komponensek, amelyek rendkívül
fontos szerepet játszanak a betegségek megelőzésében és az egészség
megőrzésében. Pozitív élettani hatásukban alapvető fontosságú, de nem
kizárólagos szerepet játszik bizonyított antioxidáns tulajdonságuk. Élettani
hatásuk pontos megismeréséhez sokkal több és megbízható, tudományosan igazolt
információra van szükségünk az élelmiszerekben előforduló flavonoidok
koncentrációjáról, a konyhatechnikai és egyéb technológiai folyamatok során
bekövetkező átalakulásokról és veszteségekről, valamint újabb epidemiológiai
tanulmányok is elengedhetetlenül szükségesek. Fentiek miatt a flavonoidok
növényi élelmiszerekkel történő rendszeres fogyasztását messzemenően javasoljuk,
amely akár a vegetárius étrend határáig is terjedhet, ugyanakkor a nagy dózisú
étrendkiegészítőkkel történő, hosszan tartó felvételt a potenciális
egészségkárosító hatások elkerülése érdekében elkerülendőnek tartjuk.
Az étrendi flavonoidok más élelmiszer-alkotókkal együtt
jutnak a szervezetbe, ezért hatásukat a kísérő, ill. jelen lévő egyéb
komponensekkel történő kölcsönhatások is befolyásolják. A flavonoidok hatása
jelenlegi ismereteink szerint főleg preventív (megelőző). Napjainkban a
flavonoidok és az egyéb polifenolos vegyületek egyre inkább a tudományos
kutatások előterébe kerülnek, mint olyan étrendi komponensek, amelyek rendkívül
fontos szerepet játszanak a betegségek megelőzésében és az egészség
megőrzésében. Pozitív élettani hatásukban alapvető fontosságú, de nem
kizárólagos szerepet játszik bizonyított antioxidáns tulajdonságuk. Élettani
hatásuk pontos megismeréséhez sokkal több és megbízható, tudományosan igazolt
információra van szükségünk az élelmiszerekben előforduló flavonoidok
koncentrációjáról, a konyhatechnikai és egyéb technológiai folyamatok során
bekövetkező átalakulásokról és veszteségekről, valamint újabb epidemiológiai
tanulmányok is elengedhetetlenül szükségesek. Fentiek miatt a flavonoidok
növényi élelmiszerekkel történő rendszeres fogyasztását messzemenően javasoljuk,
amely akár a vegetárius étrend határáig is terjedhet, ugyanakkor a nagy dózisú
étrendkiegészítőkkel történő, hosszan tartó felvételt a potenciális
egészségkárosító hatások elkerülése érdekében elkerülendőnek tartjuk.